
Ambiente, Clima e Malattie infettive – Alcune riflessioni storiche
Marzo 26, 2020Vi proponiamo di seguito un articolo interessante pubblicato sul sito Climatemonitor.it, con una brevissima ricostruzione storica di alcune delle epidemie che hanno colpito l’Europa in passato.
Buona lettura
Premessa
L’epidemiologia delle malattie infettive (Kaslov, 2014) si occupa da un lato delle circostanze che provocano il verificarsi di un’infezione e di una malattia all’interno di una popolazione (umana, animale, vegetale) e dall’altro dei fattori che influenzano frequenza, intensità, diffusione e distribuzione nello spazio e nel tempo di infezioni e malattie. L’infezione è l’ingresso e la moltiplicazione di un patogeno in un organismo ospite mentre la malattia è una risposta dell’ospite all’infezione che sia sufficientemente rilevante da dar luogo a un insieme riconoscibile di sintomi. Il verificarsi o meno dell’infezione, il manifestarsi o meno della malattia e la relativa intensità:
- Dipendono dal tipo di patogeno, dal meccanismo d’ingresso nell’ospite, dalla quantità d’inoculo e dalla suscettibilità dell’ospite, a sua volta funzione dell’età, dello stato sanitario all’atto dell’infezione, del background genetico e dello stato del sistema immunitario
- Sono influenzati dai fattori ambientali che regolano sia l’esposizione al patogeno sia la suscettibilità intrinseca e il comportamento dell’ospite. In sostanza vige il modello a triangolo che descrive l’interazione patogeno-ambiente-ospite (Scholthof, 2007) e in cui l’ambiente agisce sia sulla virulenza del patogeno sia sulla suscettibilità dell’ospite (figura 1). Del modello a triangolo esistono diverse versioni come ad esempio quella proposta da Fuhrmann (2010) e da esso emerge in modo immediato l’interesse ad analizzare come il clima[1], componente essenziale dell’ambiente, possa influenzare le malattie infettive.
Giova anche rilevare che l’epidemiologia come tutte le scienze galileiane si fonda su dati osservativi riferiti alla presenza dell’agente patogeno e della malattia in una popolazione e su modelli matematici a scopo interpretativo e predittivo. Per l’applicazione dei modelli è essenziale conoscere due fattori (Epicentro, 2009; Quan-Hui Li uet al., 2018) e cioè:
- Il tasso netto di riproduzione di un’infezione R0, che è il numero medio di nuovi casi provocati da ogni caso in una popolazione completamente suscettibile alla malattia. Si noti ad esempio che per valori di R0 superiori a 1 (ogni caso infetta più di un’altra persona) l’epidemia proseguirà nella sua fase espansiva mentre per valori di R0 inferiori all’unità l’epidemia è destinata a regredire.
- Il tempo di generazione (Tg) e cioè l’intervallo che intercorre tra l’inizio dell’infettività del caso primario e quella del caso secondario.
Da osservare inoltre che nel contesto epidemiologico i termini di endemia, epidemia e pandemia attribuiti a una malattia hanno un preciso significato.
La conoscenza più o meno dettagliata degli aspetti epidemiologici sopra delineati va ovviamente ad improntare le misure di profilassi e cura a fonte delle svariate malattie infettive che colpiscono l’uomo, gli animali e i vegetali.
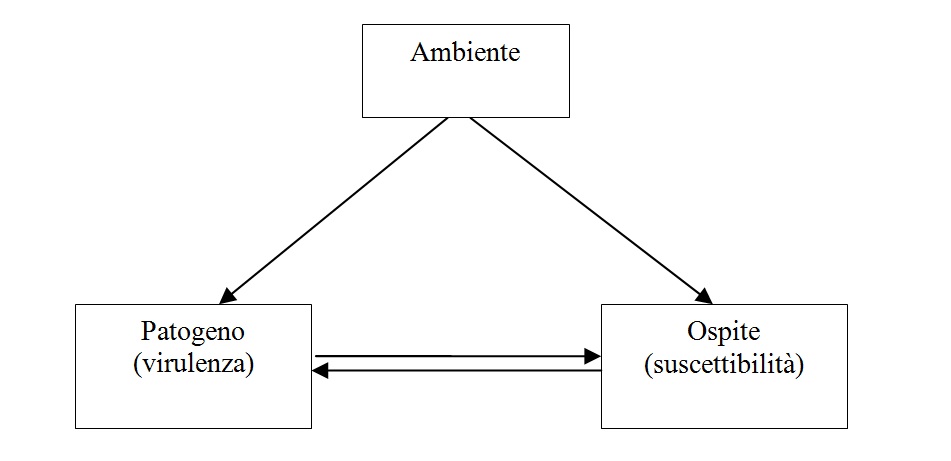
Figura 1 – Relazioni fra ambiente, ospite e patogeno. L’ambiente (nel quale un ruolo di rilievo lo hanno le condizioni meteo-climatiche) influenza sia la virulenza del patogeno sia la suscettibilità dell’ospite.
Alcune epidemie antiche
Le grandi epidemie dell’antichità ci parlano ancor oggi in modo potente attraverso testi di storici, medici, letterari e naturalisti.
A titolo di esempio si può anzitutto ricordare la peste[2] di Atene per la quale ci rimane il resoconto fattone dal generale e storico ateniese Tucidide nella Guerra del Peloponneso e poi ripreso nel De rerum natura di Lucrezio. A inizio maggio del 430 a.C., l’epidemia colpì Atene che fu poi assediata da Sparta durante la guerra del Peloponneso (431-404 a.C.). L’epidemia ebbe due picchi di mortalità nell’estate del 428 a.C. e nell’inverno del 427-426 a.C. durando in tutto 4,5-5 anni: la maggior parte della popolazione fu infettata e morirono forse 75.000 – 100.000 persone, il 25% della popolazione della città. Tucidide evidenzia come sintomi principali le eruzioni cutanee, la febbre alta e la diarrea ed evidenzia che l’epidemia si muoveva su un terreno vergine, con alti tassi d’infezione e decorso invariato in persone di età, sesso e nazionalità diverse (lo stesso statista Pericle ne morì). Nonostante la puntuale descrizione di Tucidide, sulla causa di tale epidemia non vi sono ancor oggi certezze e Littman (2009), oltre a sottolineare che l’epidemia si originò in Etiopia e si diffuse poi in tutto il Mediterraneo, ipotizza come cause più probabili il tifo, le malattie virali, la peste e il vaiolo mentre il morbillo e un’epidemia esplosiva da streptococco appaiono candidati assai meno probabili. Sempre Littman segnala anche che nel 2001 fu scoperta una fossa comune degli anni della peste e che il DNA di tifo microbico antico (Salmonella enterica serovar Typhi) è stato estratto da 3 scheletri ma poiché il tifo era endemico nel mondo greco questa non è da considerare come prova.
La peste vera e propria è dal canto suo provocata dal batterio Yersinia pestis, che ha come ospite piccoli mammiferi come ad esempio il topo nero (Rattus rattus) e infetta l’uomo attraverso insetti ematofagi (soprattutto pulci). La peste nelle due forme (bubbonica e polmonare) non è a tutt’oggi ancora del tutto debellata, come ci rammenta la World Heath Organization (WHO) e anche se gli strumenti di cura sono molto progrediti la mortalità è tuttora elevata: secondo WHO dal 2010 al 2015 a livello mondiale si sono verificati 3248 casi con 584 decessi. Per la presenza della malattia sono essenziali condizioni ambientali favorevoli alla presenza di piccoli mammiferi (in primis roditori quali i topi) e di loro parassiti ematofagi in grado di attaccare anche l’uomo. Questo spiega anche il fatto che i casi di peste siano oggi concentrati in Africa, Asia e Sud America e secondo WHO i tre paesi con più casi sono la Repubblica Democratica del Congo, il Madagascar e il Peru. In particolare in Madagascar i casi di peste bubbonica sono presenti tutto l’anno nel periodo che va da settembre ad aprile e che nel paese coincide con la stagione delle piogge.
A livello storico si devono sicuramente a Yersinia pestis:
- La peste giustinianea che colpì Bisanzio nel 542 d.C. e che è narrata da Procopio di Cesarea (Spyrou et al., 2018).
- La grande peste che giunse dall’oriente in Europa nel 1347 uccidendo più del 30% della popolazione europea (Gensini et al., 2004) e che in campo letterario si lega ad esempio alla morte della Laura di Petrarca e alla vicenda che fa da sfondo al Decameron di Boccaccio.
- La peste che infuriò in Italia nel 1630 e che a Milano causò 60.000 morti, circa la metà della popolazione (Cipolla C.M., 2005) e che è nota come peste manzoniana per il racconto che ne fa Alessandro Manzoni nei Promessi sposi e nella Storia della colonna infame.
La peste manzoniana e il ruolo della superstizione

Figura 2 – La colonna infame monumento a memoria del processo all’untore Gian Giacomo Mora posto all’angolo tra le attuali via Gian Giacomo Mora e corso di Porta Ticinese a Milano. Eretta nel 1630 dal governo milanese durante la dominazione spagnola e demolita nel 1778 durante l’amministrazione austriaca di Maria Teresa d’Austria, la colonna era intesa in origine come marchio d’infamia nei confronti dei due untori come attesta l’iscrizione che essa recava: “Qui dov’è questa piazza sorgeva un tempo la barbieria di Gian Giacomo Mora il quale congiurato con Guglielmo Piazza pubblico commissario di sanità e con altri mentre la peste infieriva più atroce sparsi qua e là mortiferi unguenti molti trasse a cruda morte. Questi due adunque giudicati nemici della patria il senato comandò che sovra alto carro martoriati prima con rovente tanaglia e tronca la mano destra si frangessero colla ruota e alla ruota intrecciati dopo sei ore scannati poscia abbruciati e perché nulla resti d’uomini così scellerati confiscati gli averi si gettassero le ceneri nel fiume. A memoria perpetua di tale reato questa casa officina del delitto il Senato medesimo ordinò spianare e giammai rialzarsi in futuro ed erigere una colonna che si appelli infame Lungi dunque, lungi da qui buoni cittadini che voi l’infelice infame suolo non contamini – Il primo d’agosto MDCXXX. (Il presidente della Pubblica Sanità, Marco Antonio Monti senatore) (Il presidente dell’ecc. Senato, Giovanni Battista Trotti) (Il R. Capitano della Giustizia, Giovanni Battista Visconti)”
Nel 1630, mentre la popolazione milanese era allo stremo per effetto della pestilenza, la situazione fu aggravata dalla superstizione popolare. Accadde ad esempio che una donna, Caterina Trocazzani Rosa, denunciò Guglielmo Piazza (ex cardatore e commissario di sanità del Ducato, che il 21 giugno 1630, durante uno dei suoi giri d’ispezione nel corso dei quali egli prendeva appunti sulla condizione degli edifici rimasti vuoti o sulle condizioni di salute delle persone, camminava rasente ai muri per proteggersi dalla pioggia) accusandolo di essere un untore che diffondeva il morbo con unguenti (l’onto pestifero) applicati ai muri e alle porte delle case. Sottoposto a tortura il povero Piazza confessò che gli unguenti erano procurati dal barbiere Gian Giacomo Mora e su tale base fu imbastito un processo in cui Piazza e Mora furono accusati di essere untori. Il procedimento, condizionato dall’impiego della tortura secondo gli usi dell’epoca, terminò con la condanna a morte dei due che confessarono la propria inesistente colpevolezza pur di porre fine alle atroci sofferenze, peraltro contraddicendo più volte le loro stesse dichiarazioni. La sentenza, oltre ad una condanna a morte eseguita il 1 agosto 1630 dopo vari supplizi inflitti sfilando per le contrade della città, prevedeva l’abbattimento della casa-bottega di Gian Giacomo Mora. Al suo posto fu installata la colonna infame, a memoria perpetua delle punizioni che sarebbero toccate a chi si fosse macchiato della colpa di essere un untore. Una narrazione più ampia della vicenda la si trova in Wikipedia alla voce “Colonna infame (Milano)”.
Da notare che la superstizione relativa agli untori persistette a lungo nell’ambiente culturale italiano, tant’è vero che:
- Nel 1713 Ludovico Muratori scriveva che «Nessun caso è più rinomato di quel di Milano, ove nel contagio del 1630, furono prese parecchie Persone, che confessarono un sì enorme delitto, e furono aspramente giustiziate. Ne esiste ivi tuttavia (e l’ho veduta anch’io) la funesta memoria nella Colonna infame posta, ov’era la Casa di quegl’inumani carnefici. Il perché grande attenzion ci vuole, affinché non si rinnovassero più simili esecrande scene»
- Nel 1738 Serviliano Latuada, nella sua Descrizione di Milano, scriveva che «Sino dall’anno 1576, in cui precedentemente la Peste aveva fatto scempio di questi Cittadini, vi furono alcuni malnati perturbatori della comune quiete, e nemici del ben pubblico, i quali o con idea di aumentare il male contagioso, o per accrescere lo spavento nel Popolo, occultamente ungevano e facevano da altri loro partitanti ungere li catenacci, ferramenti, e cantonate delle Contrade».
Essenziale fu dunque la “Storia della colonna infame”, saggio storico di Alessandro Manzoni[3], per far si che la “Colonna infame” assurgesse a simbolo della superstizione di cui Guglielmo Piazza e Gian Giacomo Mora erano state le vittime innocenti. Oggi all’angolo fra via Gian Giacomo Mora e corso di Porta Ticinese, in luogo della colonna infame vi è una scultura in bronzo con una targa che così recita: “QUI SORGEVA UN TEMPO LA CASA DI GIANGIACOMO MORA INGIUSTAMENTE TORTURATO E CONDANNATO A MORTE COME UNTORE DURANTE LA PESTILENZA DEL 1630”.
Vale la pena ricordare questi eventi anche perché la superstizione non si ripresenta mai allo stesso modo e dunque è buona cosa esser sempre vigili.
La peste nel XX secolo
Con riferimento alla peste bubbonica, ai casi reali sopra narrati si affianca la vicenda di fantasia narrata nel romanzo “La peste”, capolavoro dello scrittore francese Albert Camus, scritto nel 1947 e in cui l’autore immagina un’epidemia di peste nella città di Orano (nell’Algeria, allora colonia francese) affrontata con i mezzi propri della medicina degli anni ’40, utilizzando l’epidemia come sfondo su cui far muovere i personaggi del romanzo, in primis il medico Bernard Rieux che è il protagonista. Di particolare interesse è il brano che segue e che usando il termine peste in senso lato appare riferibile a qualsiasi epidemia:
“La parola “peste” era stata pronunciata per la prima volta. A questo punto del racconto, che lascia Bernard Rieux dietro la finestra, si concederà al narratore di giustificare l’incertezza e la meraviglia del dottore: la sua reazione, infatti, con qualche sfumatura, fu la stessa della maggior parte dei nostri concittadini. I flagelli, invero, sono una cosa comune, ma si crede difficilmente loro quando ti piombano sulla testa. Nel mondo ci sono state, in egual numero, pestilenze e guerre; e tuttavia pestilenze e guerre colgono gli uomini sempre impreparati. Il dottor Rieux era impreparato, come lo erano i nostri concittadini, e in tal modo vanno intese le sue esitazioni. In tal modo va inteso anche com’egli sia stato diviso tra l’inquietudine e la speranza. Quando scoppia una guerra, la gente dice: “Non durerà, è cosa troppo stupida”. E non vi è dubbio che una guerra sia davvero troppo stupida, ma questo non le impedisce di durare. La stupidità è sempre presente e ce ne accorgeremmo se non pensassimo sempre e solo a noi stessi. I nostri concittadini, al riguardo, erano come tutti quanti, pensavano a se stessi e in altre parole, erano umanisti e non credevano ai flagelli. Il flagello è commisurato all’uomo, ci si dice quindi che il flagello è irreale, è un brutto sogno che passerà. Ma non passa sempre, e di cattivo sogno in cattivo sogno sono gli uomini che passano, e gli umanisti in primis, in quanto non hanno preso le loro precauzioni. I nostri concittadini non erano più colpevoli d’altri, dimenticavano di essere modesti, e pensavano che tutto era ancora possibile per loro, il che presupponeva l’impossibilità dei flagelli. Continuavano a concludere affari e a preparare viaggi, avevano delle opinioni. Come avrebbero pensato alla peste, che sopprime il futuro, i mutamenti di luogo e le discussioni? Essi si credevano liberi, e nessuno sarà mai libero fintanto che ci saranno i flagelli. E persino dopo che il dottor Rieux ebbe riconosciuto davanti all’amico suo che un gruppo di malati, senza preavviso, era morto di peste, il pericolo rimaneva per lui irreale. Semplicemente, quando si è medici, ci si è fatta un’idea del dolore e si ha un po’ più di fantasia. Guardando dalla finestra la sua città che non era mutata, appena appena il dottore sentiva nascere in sé quel lieve scoramento davanti al futuro che si chiama inquietudine. Cercava di radunarsi in mente quello che sapeva della malattia. Delle cifre gli ondeggiavano nella memoria, e si diceva che la trentina di grandi pestilenze conosciute nella storia aveva fatto quasi cento milioni di morti. Ma che cosa sono cento milioni di morti? Quando si fa la guerra, appena appena si sa che cosa sia un morto. E siccome un uomo morto non ha peso che quando lo si è veduto, cento milioni di cadaveri sparsi attraverso la storia non sono che una nebbia della fantasia. Il dottore ricordava la peste di Costantinopoli che, secondo Procopio, aveva fatto diecimila vittime in un giorno. Diecimila morti fanno cinque volte il pubblico di un cinematografo. Ecco, bisognerebbe far questo: radunare le persone all’uscita di cinque cinematografi, condurle in una piazza della città e farle morire in un mucchio per vederci un po’ chiaro. Almeno, si potrebbero allora mettere dei visi noti su quel cumulo anonimo. Ma, naturalmente, è impossibile far questo; e poi, chi conosce diecimila visi?
La spagnola
Non è possibile chiudere questa breve e assai parziale rassegna storica senza parlare della pandemia influenzale nota come influenza spagnola (Spanish flu), che colpì il mondo intero tra il 1918 e il 1919 e che è senza dubbio la pandemia più grave della storia recente (CDC, 2020). L’agente causale fu il virus H1N1 che presentava geni di origine aviaria. Sebbene non vi sia ancor oggi consenso universale sul luogo d’origine del virus, sappiamo che il virus si diffuse rapidamente in tutto il mondo e si stima che un terzo della popolazione mondiale fu infettata (500 milioni di persone) e che il numero di morti fu di almeno 50 milioni. In Italia il morbo colpì oltre 4 milioni e mezzo di persone, uccidendone 410.000 nel solo 1918 e 466.000 fra 1918 e 1920, un numero impressionante se si considera che all’epoca l’Italiana aveva 36 milioni di abitanti e che 600.000 erano stati i caduti italiani nella prima guerra mondiale (Fornasin et al., 2018).
La mortalità da spagnola fu molto elevata, con picchi nelle persone di età inferiore ai 5 anni, fra 20-40 anni e oltre i 65 anni. A tale riguardo occorre rilevare che l’elevata mortalità in persone di età 20-40 anni fu una caratteristica unica di questa pandemia e ad esso non fu certo estraneo il pessimo stato sanitario delle classi che avevano fatto la grande guerra, spesso combattuta in trincea in condizioni ambientali (temperatura, umidità, stato igienico-sanitario) estreme[4].
Se le proprietà che resero l’H1N1 tanto devastante non sono fin qui state ben comprese è comunque certo che l’assenza di vaccini, di antibiotici per il trattamento delle infezioni batteriche secondarie e di antipiretici (per abbassare la febbre si ricorreva ai bagni in acqua fredda, non certo privi di conseguenze collaterali) limitò di molto gli sforzi per il contenimento della malattia, anche perché le norme di profilassi (isolamento, quarantena, buona igiene personale, uso di disinfettanti e limitazioni delle riunioni pubbliche) furono applicate in modo assai disomogeneo.
I dati sopra riportati ci invitano a riflettere sulle immani sofferenze che le pandemie del passato portarono con sé e a sviluppare una maggiore consapevolezza sul piano culturale circa le conquiste di sicurezza e civiltà che le scienze mediche hanno recato a buona parte dell’umanità (Corbellini, 2015) e il ruolo positivo giocato dalle migliorate condizioni ambientali (cibo, vestiario, abitazioni salubri).
Quarantene, lazzaretti e sanatori

Figura 4 – Robert Kock, grande scienziato ottocentesco e scopritore del bacillo della tubercolosi.
Fra i metodi di profilassi più antichi delle malattie infettive vi è la pratica della quarantena, che consiste nell’evitare il contatto della popolazione sana con individui malati. L’idea di quarantena, termine italiano da cui deriva anche l’inglese “quarantine”[5], trae origine dagli studi di Ippocrate, medico greco del V secolo a.C., il quale fissò empiricamente in 40 giorni di tempo fra l’esposizione al patogeno e la manifestazione della malattia la linea di demarcazione fra le malattie acute e quelle croniche. La prima applicazione sistematica di norme stringenti di quarantena sarebbe comunque avvenuta solo secoli dopo nella veneta Ragusa (oggi Dubrovnik), ove nel 1377 l’ufficiale sanitario Jacopo da Padova introdusse la “trentina” e cioè una quarantena della durata di un mese per i bastimenti provenienti da siti infetti o sospetti di infezione (Gensini et al., 2004).
All’idea di quarantena si associa anche quella dei lazzaretti, intesi come luoghi in cui concentrare i malati di malattie infettive per impedire il contatto con i sani. I lazzaretti si diffusero in Europa durante il Medioevo, inizialmente per ospitare i malati di lebbra, malattia che ebbe una recrudescenza in Europa a seguito delle Crociate (Bennet et al., 2008) e poi dopo la grande peste del 1348.

Figura 3 – Il medico veronese Girolamo Fracastoro (fonte: https://www.ordineinfermieribologna.it/2015/tubercolosi-tutta-la-storia-di-una-malattia-infettiva.html)
Nel XVI secolo il medico veronese Girolamo Fracastoro (1478-1553), padre dell’epidemiologia, ipotizzò che le malattie si trasmettessero attraverso particelle di minuscole dimensioni (i microbi), il che offrì una base teorica importante per quarantene e lazzaretti. Riguardo a questi ultimi non cessa di incuriosirmi il fatto che in varie città del bacino del Po essi erano realizzati ad est della città stesse (ad esempio a Milano il lazzaretto si trovava fuori della Porta Orientale – oggi Porta Venezia – e ad est di Piacenza, Parma e Bologna vi sono località dal nome evocativo di “San Lazzaro”). Ciò mi ha indotto da tempo a pensare che all’origine di tale scelta vi fosse il fatto che la circolazione atmosferica da est è meno frequente di quella da ovest ed è spesso accompagnata da pioggia, che abbatte la carica microbica dell’aria, per cui era ritenuta più bassa la possibilità che i propaguli delle malattie raggiungessero le città. Su questa mia ipotesi non dispongo però di referenze bibliografiche, per cui sarebbe interessante che qualche lettore me ne potesse segnalare.
La larga diffusione che fino agli anni ’50 del 900 ebbe una malattia batterica dall’esito spesso mortale come la tubercolosi alias TBC (il cui agente causale è Mycobacterium tuberculosis, noto anche come bacillo di Koch) spinse a creare strutture idonee alla gestione dei malati, il che spiega il sorgere di ospedali specializzati e sanatori, strutture che consentivano di isolare i malati per evitare il contagio e al contempo garantivano le condizioni in termini climatici, di igiene, alimentazione e stili di vita più idonee a contrastare la malattia in un’epoca in cui gli antibiotici non avevano ancora fatto la loro comparsa. Dati utili per un quadro cronologico delle azioni di contrasto alla TBC messe in atto in Italia fra metà ottocento e metà novecento nel più ampio contesto europeo vengono da un articolo di Martini et a. (2018) e dai dati in figura 5 da cui si apprende che nel periodo dal 1895 al 1930 la mortalità media annua da tubercolosi superò le 60000 persone, che cali sensibili si registrarono a partire dagli anni ’30 e che il trend al calo che si fece ancora più sensibile dagli anni ’50 grazie all’introduzione degli antibiotici.
Il primo sanatorio europeo fu costruito in Germania da Hermann Brehmer nel 1854 mentre in Italia il pioniere fu Biagio Castaldi, lui stesso malato di tubercolosi polmonare, che in un suo scritto del 1858 evidenziò che l’incidenza della TBC polmonare declinava col crescere della quota e la malattia era rarissima nelle popolazioni montane che vivevano oltre i 1000 m. Sulla base di ciò propose che i sanatori venissero realizzati ad alta altitudine. Negli stessi anni veniva anche evidenziato che il clima marittimo aveva un effetto positivo nella guarigione dalla tubercolosi polmonare specie se nei suoi primi stadi. Al contempo il medico Antonio Sciascia evidenziava per primo che a beneficiare dell’elioterapia erano anzitutto le forme di tubercolosi che coinvolgono i gangli linfatici, le articolazioni e ossa, la pelle, le membrane sierose e i reni.
Nei sanatori gli ospiti, oltre a essere isolati dalla comunità, godevano di un periodo di convalescenza che prevedeva escursioni all’esterno e trattamenti che comprendevano diete bilanciate, aria fresca, esposizione al sole diretto (bagni di sole) e un moderato esercizio fisico sotto controllo medico. L’architettura dei sanatori era peculiare e comprendeva stanze singole o con pochi letti e larghe terrazze. A tali principi si ispiravano strutture come ad esempio quelle di Sondalo, di Arco di Trento, di Prasomaso o quelle del Santa Corona di Garbagnate e Pietra Ligure, che negli anni hanno ospitato decine di migliaia di nostri concittadini svolgendo un ruolo insostituibile nella cura delle malattie polmonari.
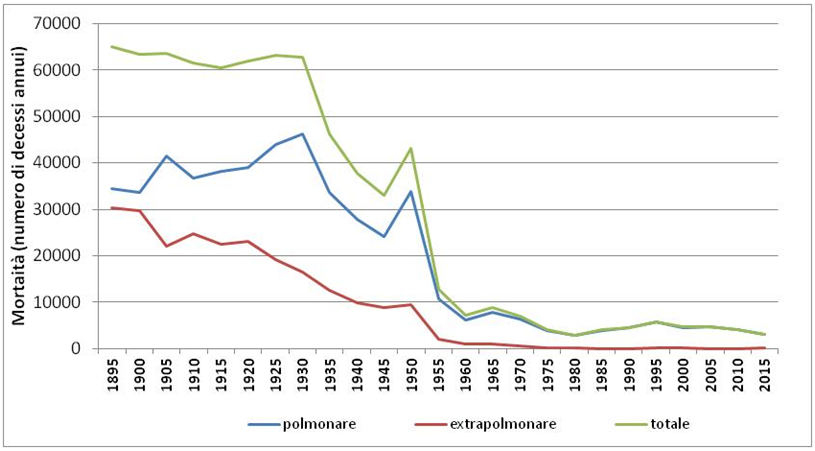
Figura 5 – Mortalità annua per 100mila abitanti dovuta a tubercolosi dal 1895 al 2015 (i dati dal 19895 al 1950 sono tratti da Ordine Infermieri Bologna, 2015; i dati dal 1955 al 2015 sono tratti da Loddo et al., 2015).
Conclusioni
Le poche vicende narrate sono comunque utili ad offrirci una seppur vaga idea del carico di sofferenze da malattie infettive che ha gravato sull’umanità fin da tempi molto antichi. Di esempi se ne sarebbero potuti offrire molti altri (penso alla malaria, alla difterite, alla meningite, alla sifilide e a tantissimi altri morbi). Peraltro il livello di conoscenza su tali fenomeni è cresciuto moltissimo grazie all’analisi genetica che ci consente oggi di individuare le tracce di microrganismi agenti delle malattie anche a distanza di migliaia di anni dal fenomeno.
A ciò si aggiungano i rimedi sopra descritti, riproposti in forma aggiornata (quarantene, controlli di frontiera, tracciamento dei contatti avuti dalle persone infette e stretta sorveglianza sull’evoluzione del fenomeno) si sono rivelati efficaci nel contrastare la pandemia del coronavirus SARS scoppiata nel 2002 e conclusasi in soli pochi mesi (Tognotti, 2013). Si tratta dei rimedi che abbiamo visto applicati con alterne fortune anche all’epidemia di COVID-19, ma questa è storia d’oggi.
Bibliografia
- Bennett B.H., Parker D.L., Robson M., 2008. Leprosy: Steps Along the Journey of Eradication, Public Health Rep. 2008 Mar-Apr; 123(2): 198–205.
- CDC, Centers for Disease Control and Prevention, 2020. 1918 Pandemic (H1N1 virus), https://www.cdc.gov/flu/pandemic-resources/1918-pandemic-h1n1.html
- Cipolla C.M., 2005. Storia economica dell’Europa pre-industriale, 2005 (p. 191).
- Corbellini C., 2015. Presentazione del libro di Eugenia Tonotti “La Spagnola in Italia, Storia dell’influenza che fece temere la fine del mondo (1918-1919)”, Franco Angeli, 2015.
- Epicentro, portale dell’epidemiologia per la sanità pubblica dell’Istituto superiore di sanità, 2009. influenza da nuovo virus A/H1N1, Notiziario – 21 maggio 2009, https://www.epicentro.iss.it/focus/h1n1/21-05-2009.Fornasin A., Breschi M., Manfredini M., 2018. Spanish flu in Italy: new data, new questions, Le Infezioni in Medicina, n. 1, 97-106.
- Fuhrmann C., 2010. The Effects of Weather and Climate on the Seasonality of Influenza, Geography Compass, 4/7 (2010): 718–730, 10.1111/j.1749-8198.2010.00343.x
- Gensini et al 2004 The concept of quarantine in history – from plague to SARS, Journal of infection, 49, 257-261.
- Kaslov A.R., 2014. Viral infections and humans, in Viral Infections of Humans: Epidemiology and Control, Richard A. Kaslow et al. (a cura di), Springer.
- Littman R.J., 2009. The plague of Athens: epidemiology and paleopathology.Mt Sinai J Med. 2009 Oct;76(5):456-67. doi: 10.1002/msj.20137
- Latuada S., 1738. Descrizione di Milano, vol. 3 (https://archive.org/details/descrizionedimil03latu/page/n10/mode/2up).
- Martini M., Gazzaniga V., Behzadifar M., Bragazzi N.L., Barberis I., 2018. The history of tuberculosis: the social role of sanatoria for the treatment of tuberculosis in Italy between the end of the 19th century and the middle of the 20th, J Prev Med Hyg 2018; 59: E323-E327.
- Ordine degli infermieri di Bologna, 2015. Tubercolosi: tutta la storia di una malattia infettiva
- https://www.ordineinfermieribologna.it/2015/tubercolosi-tutta-la-storia-di-una-malattia-infettiva.html
- Quan-Hui Liu, Ajelli M., Aleta A., Merler S., Moreno Y., Vespignan A., 2018. Measurability of the epidemic reproduction number in data-driven contact networks, Proceedings of the National Academy of Sciences, www.pnas.org/cgi/doi/10.1073/pnas.1811115115
- Scholthof K.B., 2007. The disease triangle: pathogens, the environment and society, Nat Rev Microbiol. 2007 Feb;5(2):152-6
- Spyrou M.A. et al., 2018. Analysis of 3800-year-old Yersinia pestis genomes suggests Bronze Age origin for bubonic plague, NATURE COMMUNICATIONS, (2018) 9:2234.
- Tognotti E., Lessons from the history of quarantine, from plague to influenza A, Emerging infectious diseases, Vol. 19, n.2, Febuary 2015.
- Wikipedia, 2019. Voce “Colonna infame (Milano)” https://it.wikipedia.org/wiki/Colonna_infame_(Milano)
_____________________________________________________________________________
[1] Peste in senso lato perché a produrla non fu il batterio Yersinia pestis, agente causale delle peste vera e propria.
[2] Il clima è qui inteso come l’insieme delle diverse variabili atmosferiche che agiscono alle diverse scale spazio-temporali
[3] Il Manzoni scrive fra l’altro che “… è un sollievo pensare che se non seppero quello che facevano, fu per non volerlo sapere, fu per quell’ignoranza che l’uomo assume e perde a suo piacere, e non è una scusa ma una colpa” (Alessandro Manzoni, Storia della Colonna infame).
[4] Al riguardo ricordo che nella guerra di trincea l’acqua era spesso scarsa e inquinata per cui, onde evitare malattie come il tifo, si tendeva a consumare in prevalenza vino, accompagnato da cognac prima degli assalti, il che si tradusse per molti in danni epatici permanenti. Ancora peggio se la passarono molti prigionieri di guerra. Ad esempio i nostri soldati prigionieri in Austria soffrivano di una persistente sottoalimentazione dovuta non tanto al “cattiveria del memico” quanto al fatto che le condizioni alimentari in Austria erano tremende, il che fu poi fra le cause della capitolazione degli imperi centrali. Su questo posso citare i ricordi personali di mio nonno, Luigi Mariani, che dopo il 4 novembre fu fra i soldati di scorta a un treno della croce Rossa recante aiuti alimentari per la popolazione di Vienna, stremata da 4 anni di conflitto..
[5] Quarantine non è del resto l’unico termine medico di origine italiana. Basti pensare ai termini internazionalmente noti di “influenza”, “malaria” e “pellagra” il che ci rimanda alla credibilità di cui la medicina italiana ha sempre goduto e alle piaghe che hanno afflitto per millenni la nostra popolazione.

